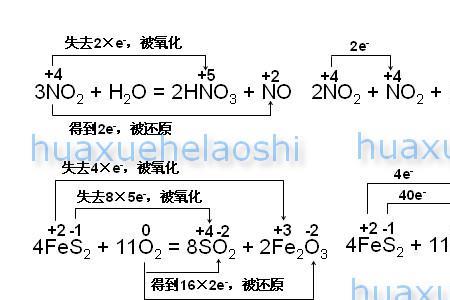
Hg+4HNO3(浓)=加热=Hg(NO3)2+2NO2+2H2O。
原理:Hg具有还原性,浓HNO3具有强氧化性,它们发生氧化还原反应。
现象:有红棕色气体产生。
解析:银比汞更不活泼,银常温下可以和稀硝酸缓慢反应(加热反应明显),那么汞的还原性比银强,也能和稀硝酸反应。由此得,浓硝酸的氧化性比稀硝酸更强,那么更易与银,汞发生氧化还原反应。液态汞加入浓硝酸后,剧烈反应,生成大量红棕色气体。汞常温液态,比起固态金属,有更大的接触面积。反应更为剧烈。气体迅速集聚,爆炸也是有一定可能性的。
浓硝酸和汞反应方程式是什么
Hg+4HNO3(浓)=加热=Hg(NO3)2+2NO2(^)+2H2O。
扩展资料:
原理:Hg具有还原性,浓HNO3具有强氧化性,它们发生氧化还原反应。现象:有红棕色气体产生。氧化-还原反应(oxidation-reductionreaction,也作redoxreaction)是化学反应前后,元素的氧化数有变化的一类反应。
氧化还原反应的实质是电子的得失或共用电子对的偏移。氧化还原反应是化学反应中的三大基本反应之一(另外两个为(路易斯)酸碱反应与自由基反应)。自然界中的燃烧,呼吸作用,光合作用,生产生活中的化学电池,金属冶炼,火箭发射等等都与氧化还原反应息息相关。
研究氧化还原反应,对人类的进步具有极其重要的意义。